Машинист крана-манипулятора 6-го разряда
Строение и свойства металлов
Материаловедение — наука, сконцентрировавшая в себе современные знания о технологиях производства и особенностях материалов и средствах их физико-химической переработки в целях изготовления деталей и изделий различного назначения.
Задачи материаловедения:
1) создание и внедрение в производство материалов для принципиально новой техники;
2) создание новых материалов и прогрессивных технологических процессов;
3) улучшение качества и ассортимента металлопродукции;
4) увеличение производства новых конструкционных материалов, покрытий и изделий на основе металлических порошков;
5) развитие производства новых полимерных и композиционных материалов с комплексом заданных свойств;
6) обеспечение более широкого применения малоотходных, безотходных и малооперационных технологических процессов;
7) увеличение использования высокоэффективных методов обработки металлов и материалов, обеспечивающих существенное улучшение их свойств, и др.
В настоящее время материаловедение подразделяют на технологию металлов, технологию древесных материалов, технологию пластических масс и других материалов.
Достоинством металлов и сплавов является то, что путем целенаправленного изменения их химического состава и внутреннего строения можно получать различные конструкционные материалы с новыми свойствами, дающими возможность применения их во всех отраслях народного хозяйства.
Используемые в технике металлы принято подразделять на две основные группы — черные и цветные. К черным металлам относят железо и его сплавы (чугун, сталь, ферросплавы). Остальные металлы и их сплавы составляют группу цветных.
Достоинствами неметаллических материалов являются стойкость к коррозионному износу, небольшая по сравнению с металлами масса и другие специфические свойства.
Прикладную науку о строении и свойствах технических материалов, основной задачей которой является установление связи между составом, структурой и свойствами, называют материаловедением. Из металлов особое значение имеют железо и его сплавы, являющиеся до настоящего времени основным машиностроительным материалом. Результаты исследований материаловедения используются во всех отраслях народного хозяйства: в станкостроении, судостроении, автомобильной и авиационной промышленности, электронике и радиотехнике и др.
Черные металлы представляют собой сплав железа с углеродом. Кроме углерода черные металлы в небольшом количестве могут содержать кремний, марганец, фосфор, серу и другие химические элементы. Для придания черным металлам специфических свойств к ним добавляют некоторые так называемые легирующие вещества — медь, никель, хром и др. Черные металлы в зависимости от содержания углерода подразделяют на чугуны и стали.
Чугун представляет собой сплав железа и углерода 2…4,3%. В специальных чугунах — ферросплавах — количество углерода может достигать 5% и более. Присутствующие в чугуне кремний, марганец, фосфор и сера существенно влияют на его свойства: сера и фосфор повышают хрупкость чугуна, а специальная присадка хрома, никеля, магния, алюминия и кремния придает чугуну более высокие жаростойкость, износостойкость, повышенную сопротивляемость коррозии. Чугуны с добавкой указанных веществ называются легированными. В зависимости от формы, в которой углерод находится в чугуне, различают чугуны серые (литейные) и белые (передельные). В серых чугунах углерод находится в свободном состоянии в виде графита, а в белом — в связанном состоянии в виде цемента. Пластинки графита, перерезающие металлическую структуру чугуна, понижают его прочность. Модифицированный серый чугун имеет более высокие механические свойства благодаря шаровидной и раздробленной форме графита.
Сталь содержит углерода до 2%. В отличие от чугуна — хрупкого металла — сталь пластична, упруга и обладает высокими технологическими свойствами (способностью обрабатываться). В зависимости от назначения различают стали конструкционные, содержащие 0,02…0,85% углерода, и инструментальные — 0,65…1,4%. Конструкционные стали, применяемые для строительных конструкций и арматуры железобетона, а также в машиностроении, обладают хорошей пластичностью, низкой хрупкостью. Повышение же углерода в инструментальных сталях придает им высокую твердость и хрупкость.
Механические и физические свойства сталей (жаростойкость, износостойкость, коррозионная стойкость) повышаются добавкой к ним никеля, хрома, вольфрама, молибдена, кобальта, меди, алюминия и др., называемых легирующими веществами, а стали — легированными. В зависимости от величины легирующих добавок различают стали низколегированные, содержащие до 2% легирующих веществ, среднелегированные — 2…10% и высоколегированные — более 10%. Строители широко применяют низколегированную сталь. Нержавеющая сталь является высоколегированной.
Цветные металлы и сплавы подразделяются по плотности на легкие и тяжелые. К легким относятся сплавы на основе алюминия, магния, а к тяжелым — на основе меди, никеля, олова, свинца. За последние годы в технологии металлургии внедрены новые усовершенствования: освоен эффективный метод вакуумной обработки живой стали; получены новые виды высокопрочных сталей и чугунов; разработана эффективная технология получения алюминия из нефелинов; освоены новые виды облегченного проката, гнутого из лент и полос, диффузионный метод сварки металлов в вакууме, легирование с вакуумной обработкой, широко развивается порошковая металлургия.
Строение металлов и их свойства.
Металлы и металлические сплавы представляют собой кристаллические тела, состоящие из бесчисленного множества кристаллических образований, групп (в виде отдельных прочно связанных между собой зерен. Большинство их имеет кубическую объемно центрипованную (хром, ванадий, молибден, вольфрам и некоторые другие) и кубическую гранецентрированную решетки (алюминий медь, никель, свинец, золото и серебро). Железо может быть в нескольких кристаллических формах с различным расположением атомов. Это явление называется аллотропией. Аллотропические превращения железа наблюдаются при изменении температуры.
Железо из расплавленной массы кристаллизуется в форме решетки объемно центрированного куба; при охлаждении до температуры 1390°С она перекристаллизовывается в решетку гранецентрированного куба, а при 898°С снова образует решетку объемно центрированного куба и а-модификации. Аллотропия железа имеет большое значение в процессах горячей механической и термической обработки чугуна и стали. Регулируя закалкой, отжигом и другими способами содержание этих модификаций в сталях, придают им заданные механические свойства.
При затвердевании расплава металла вначале образуются мельчайшие кристаллы правильной формы, затем, по мере охлаждения, они увеличиваются в размерах и срастаются между собой в виде деформированных неправильной внешней формы кристаллов, называемых кристаллитами. Их хорошо видно под микроскопом.
Физические свойства металлов и сплавов характеризуются цветом, плотностью, температурой плавления, теплопроводностью, коэффициентом температурного расширения. Плотность большинства металлов превышает 7000 кг/м3, а плотность легких металлов (алюминия, бериллия, магния) менее 3000 кг/м3. Чем меньше плотность металла, тем легче и эффективнее оказываются строительные конструкции из него. Вот почему конструкции из сплавов на основе алюминия все шире применяются в строительстве.
Температуру плавления металлов важно знать для выбора режима горячей обработки металлов и получения изделий литьем. Температура плавления металла изменяется при добавке к нему других веществ. Большинство сплавов, например на основе железа, имеют температуру плавления ниже, чем входное в их состав металлы. Однако некоторые сплавы цветных еталлов, например никеля и алюминия, имеют более высокую температуру плавления, чем чистый никель и алюминий. Изменение температуры плавления металла от содержания в нем других веществ характеризуется диаграммой состояния.
Расширение металлов при нагревании характеризуется коэффициентом линейного и объемного расширения. Это свойство металла необходимо учитывать при проектировании металлических строительных конструкций, так как последние под действием изменяющейся температуры могут вызвать разрушение сооружения. Важно учитывать это свойство металла при сварке, так как в результате местного нагрева свариваемых деталей может произойти образование трещин. Способность металла удлиняться при нагревании эффективно используется при производстве предварительно напряженных железобетонных изделий способом электротермического натяжения арматуры.
Механические свойства металлов характеризуются их прочностью, твердостью, ударной вязкостью, усталостью и ползучестью.
Прочность — это способность металла или сплава сопротивляться действию внешних сил. В зависимости от характера этих сил различают прочность при растяжении, сжатии, изгибе, кручении. Характеризуются они соответствующим пределом прочности, т. е. условным напряжением, при котором испытуемый образец металла разрушается.
Универсально испытание на растяжение, применяемое для всех металлов и сплавов. Специфическим, например, для серого чугуна, является испытание при сжатии и изгибе. При испытании металлов при растяжении определяют предел текучести — напряжение, при котором растяжение образца происходит без увеличения растягивающей нагрузки. Этот показатель служит основным при расчете металлических конструкций.
На усталость, или выносливость, испытывают образцы из стали и цветных тяжелых и легких сплавов, детали из которых работают в условиях повторно-переменных растягивающих, изгибающих, сжимающих, крутящих и других нагрузок.
На ползучесть, т. е. способность деформироваться под постоянной нагрузкой, испытывают металлы, непрерывно работающие под напряжением. В результате ползучести могут увеличиваться прогибы строительных конструкций, произойти потеря устойчивости. Особенно опасна ползучесть арматурной стали в предварительно напряженных железобетонных конструкциях. Как результат ее, могут произойти потеря предварительного напряжения арматуры, образование трещин в бетоне и разрушение конструкции. Твердость металла определяет противодействие его при вдавливании в него твердого стального шарика (метод Бринелля), алмазного корпуса или алмазной пирамиды.
Вязкость различают статическую и ударную (динамическую). Статическая вязкость характеризуется относительным удлинением (в процентах длины образца при разрыве) к его первоначальной длине, а ударная вязкость — количеством работы потребной для разрушения образца ударной нагрузкой.
Технологические свойства характеризуют способность металла подвергаться обработке. К ним относятся: пластичность, позволяющая получать металлические изделия ковкой, прокаткой волочением; обрабатываемость резанием; свариваемость, характеризуемая способностью металла давать прочные соединения путем их местного нагрева до пластичного или жидкого состояния.
Классификация сталей
Стали классифицируют по назначению для дальнейшего использования, химическому составу, качеству, структуре.
По назначению стали принято делить на конструкционные, коррозионно стойкие (нержавеющие), инструментальные, жаропрочные, криогенные.
- Легированная — сталь содержащая специально вводимые, в определённых количествах, элементы, которые обеспечивают требуемые физические или механические свойства. Эти элементы называются легирующими. Как правило, легирование повышает прочность, коррозийную стойкость стали, понижают хрупкость. Легированную сталь по степени легирования разделяют на: низколегированную (легирующих элементов до 2,5 %); среднелегированную (от 2,5 до 10 %); высоколегированную (от 10 до 50 %).
- Конструкционная — сталь применяемая при изготовлении различных деталей, механизмов и конструкций в машиностроении и строительстве, обладающая определёнными механическими, физическими и химическими свойствами.
- Нержавеющая — легированная сталь, устойчивая к коррозии в атмосфере и агрессивных средах.
- Инструментальная углеродистая — сталь с содержанием углерода от 0,7 % и выше. Она отличается высокой твёрдостью и прочностью и применяется для изготовления инструмента.
- Жаропрочная — это вид стали, который подлежит эксплуатации при высоких температурах (от 30% от температуры плавления).
По химическому составу стали делятся на углеродистые и легированные.
Углеродистые стали по уровню содержания углерода, в свою очередь, делятся на: низкоуглеродистые (процент содержания углерода до 0,25%), среднеуглеродистые (0,3–0,55%) и высокоуглеродистые (0,6–2 %). Углерод придаёт сплавам из железа дополнительную прочность и твёрдость, но, при этом, понижая их пластичность и вязкость.
Углеродистая сталь обыкновенного качества
Углеродистая сталь обыкновенного качества содержит углерод в пределах 0,06–0,49%. К этой группе относятся следующие марки стали: Ст1, Ст2, Ст3, Ст4, Ст5, Ст6, Ст0. По химическому составу данный тип стали должен соответствовать ГОСТ 380-94, а производимый из нее металлопрокат должен соответствовать общим техническими условиями ГОСТ 535-2005.
Чаще всего для изготовления металлопродукции используется сталь марки Ст3сп/пс1-5: из нее изготавливается сортовой, фасонный, листовой и рулонный прокат, а также горячекатаные трубы.
Качественная углеродистая сталь
Низкоуглеродистая качественная конструкционная сталь (марки 08, 08кп, 08пс) — используется при изготовлении листового проката. Это мягкая сталь, и она легко обрабатывается штамповкой, давлением, профилированием.
Качественная конструкционная сталь (марки 10, 15, 20, 25) — используется при изготовлении стальных труб, в машиностроении. Она обладает более высокой прочностью и коррозеустойчивостью по сравнению с маркой Ст3.
Твердая качественная сталь (марки 30, 35, 40, 45) — используется в машиностроении при изготовлении сильно нагруженных деталей машин. Эти марки стали обладают высокой износостойкостью и еще более устойчивы к коррозии.
Для улучшения характеристик сталей применяют ее легирование. Цели легирования — это повышение: прочности, устойчивости против коррозии, термостойкость, жаропрочность и т.д.
Легирование — это процесс добавление в состав материалов примесей, вводимых для изменения свойств основного материала.
Легированные стали по уровню содержания легирующих элементов делятся на низколегированные (до 4%), среднелегированные (до 11%) и высоколегированные (более 11%).
Стали, в зависимости от технологии их производства, могут содержать разное количество примесей.
Уровень содержания примесей определят (классифицирует) качество стали: обыкновенного качества, качественные, высококачественные и особо высококачественные.
По структуре стали разделяются на аустенитную, ферритную, мартенситную, бейнитную и перлитную и двухфазную и многофазную.
Производство стали заключается в переработке чугуна, при котором в чугуне уменьшается концентрация углерода и других ненужных примесей.
Физические и химические свойства стали определяется ее составом и структурой, которые зависят от присутствия и процентного содержания следующих основных составляющих:
- Углерод — элемент увеличение содержания которого увеличивает твердость и прочность стали уменьшая ее пластичность.
- Сера — вредная примесь, которая влияет на ломкость стали, уменьшает пластичность и прочность стали, износостойкость и коррозионную стойкость.
- Фосфор — вредная примесь, которая влияет на хладноломкость (хрупкость при пониженных температурах) стали.
- Феррит — примесь, которая придает стали мягкость и пластичность.
- Цементит — примесь, которая придает стали твердость и хрупкость.
- Кремний и марганец, при процентном содержании порядка 0,5–0,7% значимого влияния на свойства стали не оказывают.
Не прошедшая обработку сталь очень пластична, её можно обрабатывать путем деформирования: ковка, вальцовка, штамповка.
Кристаллическое строение металлов
Все металлы и металлические сплавы − тела кристаллические, атомы (ионы) расположены в металлах закономерно в отличие от аморфных тел, в которых атомы расположены хаотично. Металлы (если их получают обычным способом) представляют собой поликристаллические тела, состоящие из большого числа мелких (10 в минус 1 степени…10 в минус 4 степени см), различно ориентированных по отношению друг к другу кристаллов. В процессе кристаллизации они приобретают неправильную форму и называются кристаллитами, или зернами. Металлы в твердом и отчасти в жидком состояниях обладают
рядом характерных свойств:
• высокими теплопроводностью и электрической проводимостью;
• положительным температурным коэффициентом электрического сопротивления; с повышением температуры электрическое сопротивление чистых металлов возрастает; большое число металлов (~30) обладает сверхпроводимостью (у этих металлов при температуре, близкой к абсолютному нулю, электрическое сопротивление падает скачкообразно, практически до нуля);
• термоэлектронной эмиссией, т.е. способностью испускать электроны при нагреве;
• хорошей отражательной способностью: металлы непрозрачны и обладают металлическим блеском;
• повышенной способностью к пластической деформации.
Наличие этих свойств и характеризует так называемое металлическое состояние веществ. Чистые металлы в обычном структурном состоянии обладают
низкой прочностью и не обеспечивают во многих случаях требуемых свойств, поэтому они применяются сравнительно редко. Наиболее широко используются сплавы, которые получают сплавлением или спеканием порошков двух или более металлов или металлов с неметаллами. Они обладают характерными свойствами, присущими металлическому состоянию. Химические элементы, образующие сплав, называют компонентами. Сплав может состоять из двух или большего числа компонентов. В металловедении широко используются понятия «система», «фаза», «структура». Совокупность фаз, находящихся в состоянии
равновесия, называют системой. Фазой называют однородные (гомогенные) составные части системы, имеющие одинаковый состав, кристаллическое строение и свойства, одно и то же агрегатное состояние и отделенные от составных частей поверхностями раздела. Под структурой понимают форму, размеры и характер взаимного расположения соответствующих фаз в металлах и сплавах.
Структурными составляющими сплава называют обособленные части сплава, имеющие одинаковое строение с присущими им характерными особенностями.
Различают макроструктуру (строение металла или сплава, видимое невооруженным глазом или при небольшом увеличении в 30 – 40 раз) и микроструктуру (строение металла или сплава, наблюдаемое с помощью микроскопа при больших увеличениях). Макроструктуру исследуют на специальных макрошлифах
(темплетах). Для приготовления макрошлифа образцы вырезают из крупных заготовок (слитков, поковок и т. д.) или изделий, поверхность которых шлифуют, полируют, а затем подвергают травлению специальными реактивами. При исследовании макрошлифа можно обнаружить форму и расположение зерен в литом металле (рис. 1, а, б); волокна (деформированные кристаллиты) в поковках и штамповых заготовках (рис. 1, в), дефекты, нарушающие сплошность металла (усадочную рыхлость, газовые пузыри, раковины, трещины и т. д.); химическую неоднородность сплава, вызванную процессом кристаллизации или
созданную термической или химико-термической (цементация, азотирование и т. д.) обработкой.

Микроструктура показывает (рис. 2, а, б) размер и форму зерен, взаимное расположение фаз, их форму и размеры. Для определения микроструктуры из исследуемого металла изготовляют микрошлиф, т. е. небольшой образец, одну из плоскостей которого тщательно шлифуют, полируют и подвергают травлению специальными реактивами. Микроструктуру металлов наблюдают в микроскопе − оптическом или электронном. Разрешающая способность оптического микроскопа, т.е. минимальная величина объекта (детали структуры), которая различима с его помощью, не превышает 0,2 мкм (200 нм). Полезное увеличение в оптическом микроскопе достигает примерно 2000 раз.

Атомно-кристаллическая структура металлов
Под атомно-кристаллической структурой понимают взаимное расположение атомов (ионов), существующее в реальном кристалле. В твердом состоянии металл представляет собой постройку, состоящую из положительно заряженных ионов, омываемых “газом” из свободных коллективизированных электронов. Связь в металле осуществляется электростатическими силами. Между ионами и коллективизированными электронами проводимости возникают электростатические силы притяжения, которые стягивают ионы. Такая связь называется металлической.
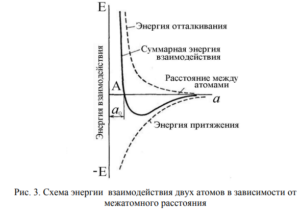
Силы связи в металлах определяются силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстоянии один от другого, при котором энергия взаимодействия минимальна. Как видно из рис. 3, этому положению соответствует равновесное расстояние
![]() Сближение атомов (ионов) на расстояние, меньшее ао, или удаление их на расстояние, большее
Сближение атомов (ионов) на расстояние, меньшее ао, или удаление их на расстояние, большее ![]() осуществимо лишь при совершении определенной
осуществимо лишь при совершении определенной
работы против сил отталкивания и притяжения. Поэтому в металле атомы располагаются закономерно, образуя правильную кристаллическую решетку, что соответствует минимальной энергии взаимодействия атомов. Кристаллическая решетка (рис. 4) состоит из воображаемых линий и плоскостей, проходящих через точки расположения ионов в пространстве. В случае двухмерного изображения элементарная ячейка будет представлять собой плоский атомный узор в виде параллелограмма, в трехмерном пространстве она будет изображаться параллелепипедом. Жирными линиями выведен наименьший параллелепипед, последовательным перемещением которого вдоль трех своих осей может быть построен весь кристалл.
В результате весь кристалл можно составить, подгоняя друг к другу такие идентичные блоки, как элементарные ячейки. Этот наименьший объем кристалла, дающий представление об атомной структуре металла в любом объеме, получил название элементарной кристаллической ячейки.

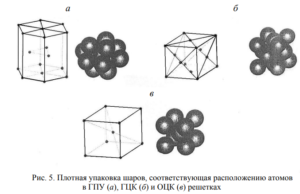
Для однозначной ее характеристики необходимо знать следующие величины: три ребра (a, b и c) и три угла между осями α, β и γ (рис. 4). Большинство металлов образует одну из следующих высокосимметричных решеток с плотной упаковкой атомов: кубическую объемноцентрированную, кубическую гранецентрированную и гексагональную (рис. 5). Как видно из рис. 5, в, в кубической объемноцентрированной решетке (ОЦК) атомы расположены в вершинах куба и один атомов центре объема куба. Кубическую объемноцентрированную решетку имеют металлы: Рb, К, Na, Li, Tiβ, Zrβ, Та, W, V, Feα, Cr, Nb, Ва и др.
В кубической гранецентрированной решетке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани (рис. 5, б). Решетку такого типа имеют металлы: Саα, Се, Srα, Tn, Ni, Ag, Аи, Pd, Pt, Rh, Jr, Feγ, Си, Coα и др. В гексагональной решетке (рис. 5, а) атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома − в средней плоскости призмы. Такую упаковку атомов имеют металлы: Mg, Tiα, Cd, Re, Os, Ru, Zn, Coβ, Be, Саβ и др.
Расстояния a, b, с между центрами ближайших атомов в элементарной ячейке (см. рис. 5) называются периодами решетки. Период решетки выражается в нанометрах. Периоды решетки для большинства металлов находятся в пределах 0,1 – 0,7 нм.
На одну элементарную ячейку объемноцентрированной решетки приходятся два атома: один в центре куба и другой вносят атомы, располагающиеся в вершинах куба (каждый атом в вершине куба одновременно принадлежит восьми сопряженным элементарным ячейкам и на данную ячейку приходится лишь 1/8 массы этого атома, а на всю ячейку (1/8) × 8 = 1 атом). На элементарную ячейку гранецентрированной кубической решетки приходятся четыре атома; из них один (по такому же расчету, как и для объемноцентрированной кубической решетки) вносят атомы в вершинах куба, а три суммарно ((1/2) × 6 = 3) вносят атомы, находящиеся на середине грани, так как каждый из таких атомов принадлежит двум решеткам.
На элементарную ячейку гексагональной плотноупакованной решетки приходятся шесть атомов (3 + (1/6) × 12 + (1/2) × 2 = 6). Плотность кристаллической решетки − объема, занятого атомами, которые условно можно рассматривать как жесткие шары (см. рис. 6, а), характеризуется координационным числом, под которым понимают число атомов, находящихся на равном и наименьшем расстоянии от данного атома. Чем выше координационное число, тем больше плотность упаковки атомов.
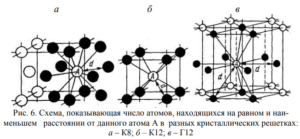
В элементарной ячейке объемноцентрированной кубической решетки наименьшее расстояние между атомами соответствует ![]() На этом расстоянии от данного атома находятся 8 соседей (рис. 6, а). Следовательно, координационное число для ОЦК решетки соответствует 8 и обозначается К8. Коэффициент компактности ячейки, определяемый как отношение объема, занятого атомами, к объему ячейки составляет для ОЦК решетки 68 %. Для гранецентрированной кубической решетки координационное число равно 12 (К12); каждый атом имеет 12 ближайших соседей на расстоянии
На этом расстоянии от данного атома находятся 8 соседей (рис. 6, а). Следовательно, координационное число для ОЦК решетки соответствует 8 и обозначается К8. Коэффициент компактности ячейки, определяемый как отношение объема, занятого атомами, к объему ячейки составляет для ОЦК решетки 68 %. Для гранецентрированной кубической решетки координационное число равно 12 (К12); каждый атом имеет 12 ближайших соседей на расстоянии ![]()
(рис. 6, б), что соответствует наибольшей плотности упаковки или укладки в виде шаров. Гексагональная плотноупакованная решетка, для которой с/а = 1,633 (например Мg и Co), имеет координационное число 12 (К12), что также соответствует наибольшей плотности упаковки шаров (атомов) (рис. 7, в). У многих металлов, кристаллизующихся в гексагональной системе, отношение с/а находится в пределах 1,57 – 1,64, т. е. может отклоняться от плотнейшей упаковки, при которой с/а = 1,633. Если отношение с/а значительно отличается от 1,633 (например, для цинка и кадмия с/а> 1,633), то координационное число гексагональной решетки соответствует 6. При расположении атомов малой осью вдоль z отношение с/а< 1,633 ![]()
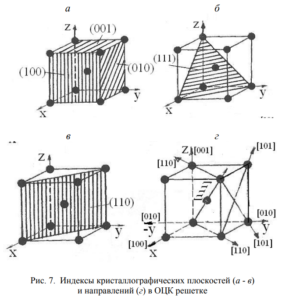
Гранецентрированная кубическая и гексагональная плотноупакованная (с/а = 1,633) решетки − наиболее компактные; в них коэффициент компактности равен 74 %. Кристаллографические обозначения атомных плоскостей. Для определения положения атомных плоскостей (проходящих через атомы) в кристаллических пространственных решетках пользуются индексами (h k l), представляющими собой три целых рациональных числа, являющихся величинами, обратными отрезкам осей, отсекаемым данной плоскостью на осях координат. Единицы длины вдоль осей выбирают равными длине ребер элементарной ячейки. Эти числа заключают в круглые скобки.
Приведем примеры обозначения плоскостей. Установим первоначально индексы для плоскости куба. Каждая плоскость куба пересекает только одну ось (рис. 7, а), при этом отсекаемые отрезки будут равны (1, ∞, ∞); (∞, 1, ∞); (∞, ∞, 1).
Обратные величины отсекаемых отрезков будут соответственно равны: (1, 0, 0); (0, 1, 0); (0, 0, 1).

Следует иметь в виду, что индексы характеризуют не одну какую-либо плоскость, а целую группу параллельных плоскостей. Совокупность однотипных эквивалентных плоскостей заключают в фигурные скобки. Индексы направлений. Индексы направлений [u v w] −это три целых простых числа, являющиеся координатами узла от ближайшего начала ординат и расположенного на этом направлении. Для определения индексов направлений расположения рядов атомов в кристаллической решетке необходимо из семейства параллельных плоскостей выбрать направление плоскостей, проходящих через начало координат. Далее, приняв за единицу длину ребра элементарной ячейки (или период решетки), определяют координаты любой точки этого направления. Полученные значения координат точки приводят к отношению трех наименьших чисел. Эти числа, заключенные в квадратные скобки [u v w], являются индексами данного направления и всех параллельных ему направлений.
Основные направления в кубической решетке приведены на рис. 7, г. Индексы осей решетки х − [100], у − [010] и z − [001]. Индексы пространственной диагонали [111]. Для кубической решетки индексы направлений [u v w], перпендикулярных к плоскости (h k l), численно равны индексам этой плоскости. Например, индексы оси x равны [100], а индексы плоскости, перпендикулярной к оси х, равны (100).
Анизотропия свойств металлов. Можно заметить, что плотность расположения атомов по различным плоскостям (так называемая ретикулярная плотность) неодинакова. Так, плоскости (100) в ОЦК решетке принадлежит лишь один атом ((1/4) × 4), плоскости ромбического додекаэдра (110) − два атома: один атом вносят атомы, находящиеся в вершинах [(1/4) × 4], и один атом в центре куба. В ГЦК решетке плоскостью с наиболее плотным расположением атомов будет плоскость октаэдра (111), а в ОЦК решетке − плоскость (110). Вследствие неодинаковой плотности атомов в различных плоскостях и направлениях решетки свойства (химические, физические, механические) каждого монокристалла зависят от направления вырезки образца по отношению к направлениям в решетке. Подобная неодинаковость свойств монокристалла в разных направлениях называется анизотропией.
Дефекты кристаллов
Строение реальных кристаллов отличается от идеальных. В реальных кристаллах всегда содержатся дефекты, которые подразделяют на точечные, линейные, поверхностные и объемные. Размеры точечного дефекта близки к межатомному расстоянию. У линейных дефектов длина на несколько порядков больше ширины; у поверхностных дефектов мала толщина, а ширина и длина больше ее на несколько порядков. Объемные дефекты (поры, трещины) имеют значительные размеры во всех трех направлениях. Дефекты сохраняют подвижность, способны перемещаться в кристаллической решетке и при сближении взаимодействуют между собой. В большинстве случаев подвижность дефектов контролируется диффузией. Передвижение дислокаций под действием напряжений не связано с массопереносом, дислокации подвижны и при низких температурах, когда диффузия уже не играет никакой роли. К самым
простым точечным дефектам относятся вакансии, межузельные атомы основного вещества, чужеродные атомы внедрения (рис. 8).
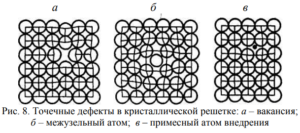
Вакансией называется пустой узел кристаллической решетки, а межузельным атомом – атом, перемещенный из узла в позицию между узлами.
Вакансии и межузельные атомы появляются в кристаллах при любой температуре выше абсолютного нуля из-за тепловых колебаний атомов. Каждой температуре соответствует равновесная концентрация вакансий, а также межузельных атомов. Пересыщение точечными дефектами достигается при резком
охлаждении после высокотемпературного нагрева, при пластическом деформировании и при облучении нейтронами. В последнем случае концентрация вакансий и межузельных атомов одинакова: выбитые из узлов решетки атомы становятся межузельными атомами, а освободившиеся узлы становятся вакансиями.
С течением времени избыток вакансий сверх равновесной концентрации уничтожается на свободных поверхностях кристалла, порах, границах зерен и других дефектах решетки. Места, где исчезают вакансии, называются стоками вакансий. Вакансии являются самой важной разновидностью точечных дефектов; они ускоряют все процессы, связанные с перемещениями атомов (диффузия, спекание порошков и т. д.). Все виды точечных дефектов искажают кристаллическую решетку и в определенной мере влияют на физические свойства. В технически чистых металлах точечные дефекты повышают электросопротивление, а на механические свойства почти не влияют. Лишь при больших концентрациях дефектов в облученных металлах понижается пластичность и заметно изменяются другие свойства.
Важнейшие виды линейных несовершенств – краевые и винтовые дислокации (рис. 9). Краевая дислокация в сечении представляет собой край «лишней» полуплоскости в решетке (см. рис. 9, а, б). Вокруг дислокаций решетка упруго искажена. Мерой искажения служит так называемый вектор Бюргерса. Он
получается, если обойти замкнутый контур в идеальном кристалле (рис. 10, а, б), переходя от узла к узлу, а затем этот же путь повторить в реальном кристалле, заключив дислокацию внутрь контура. Как видно на рис. 10, б, в реальном кристалле контур окажется незамкнутым. Вектор b, который нужен для замыкания контура, называется вектором Бюргерса. У краевой дислокации вектор Бюргерса равен межатомному расстоянию и перпендикулярен дислокационной линии, у винтовой дислокации − параллелен ей. Полные дислокации легко перемещаются под действием напряжений в отличие от частичных дислокаций, у которых вектор Бюргерса меньше межатомного расстояния.

Плотность дислокаций − это суммарная длина всех линий дислокаций в единице объема. В полупроводниковых кристаллах она равна ![]() , у отожженных металлов –
, у отожженных металлов – ![]() . При холодном пластическом деформировании плотность дислокаций возрастает до
. При холодном пластическом деформировании плотность дислокаций возрастает до ![]() . Попытка увеличить плотность свыше
. Попытка увеличить плотность свыше ![]() быстро приводит к появлению трещин и разрушению металла. Дислокации возникают при кристаллизации, плотность их большая, поэтому они значительно влияют на свойства материалов. Дислокации наряду с другими дефектами участвуют в фазовых превращениях.
быстро приводит к появлению трещин и разрушению металла. Дислокации возникают при кристаллизации, плотность их большая, поэтому они значительно влияют на свойства материалов. Дислокации наряду с другими дефектами участвуют в фазовых превращениях.
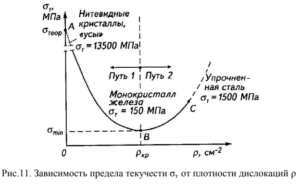
Примесные атомы образуют вокруг дислокации зону повышенной концентрации – так называемую атмосферу Коттрелла, которая мешает движению дислокаций и упрочняет металл. Прочность бездефектных участков (в том числе длинных и тонких «усов», полученных кристаллизацией из газовой фазы) приближается к теоретической (рис. 11).
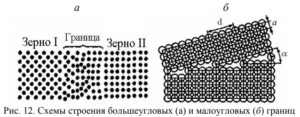
Наиболее важными поверхностными дефектами являются большеугловые и малоугловые границы, дефекты упаковки, границы двойников. Поликристаллический сплав содержит огромное число мелких зерен. В соседних зернах решетки ориентированы различно (рис. 12), и граница между зернами представляет собой переходный слой шириной 1 – 5 нм. В нем нарушена правильность расположения атомов, имеются скопления дислокаций, повышена концентрация примесей. Границы между зернами называются болыиеугловыми, так как соответственные кристаллографические направления в соседних зернах образуют углы в десятки градусов (рис. 12, а).
Каждое зерно, в свою очередь, состоит из субзерен (блоков). Субзерно представляет собой часть кристалла относительно правильного строения, а его границы – стенки дислокаций, которые разделяют зерно на отдельные субзерна (рис. 12, б). Угол взаимной разориентации между соседними субзернами невелик (не более 5°), поэтому такие границы называются малоугловыми. На малоугловых границах также скапливаются примеси. Дефект упаковки представляет собой часть атомной плоскости, ограненную дислокациями, в пределах которой нарушен нормальный порядок чередования атомных слоев. Например, в сплавах с ГЦК решеткой чередуются плотноупакованные слои АВСАВСАВ…, а при прохождении через дефект упаковки слои чередуются в последовательности АВCBCABC… Поверхностные дефекты влияют на механические и физические свойства материалов. Особенно большое значение имеют границы зерен. Предел текучести σт связан с размером зерна зависимостью:

![]()
Чем мельче зерно, тем выше предел текучести, вязкость и меньше опасность хрупкого разрушения. Аналогично, но более слабо влияет на механические свойства размер субзерен.
Вдоль границ зерен и субзерен быстро протекает диффузия (во много раз быстрее, чем сквозь кристалл) особенно при нагреве. Взаимодействие между дефектами, перемещение их в кристаллах, изменение концентрации дефектов − все это отражается на свойствах и имеет большое практическое значение.
Кристаллизация чистых металлов
Переход металла из жидкого состояния в твердое (кристаллическое) называется кристаллизацией. В жидком металле сохраняется так называемый ближний порядок, когда упорядоченное расположение атомов распространяется на небольшое расстояние. Вследствие интенсивного теплового движения атомов ближний порядок неустойчив. Кристаллизация состоит из двух одновременно идущих процессов − зарождения и роста кристаллов. Кристаллы могут зарождаться самопроизвольно – самопроизвольная кристаллизация или расти на имеющихся готовых центрах кристаллизации – несамопроизвольная
кристаллизация. Самопроизвольная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние. Кристаллизация протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию с меньшей энергией Гиббса (свободной энергией) G, т. е. когда энергия Гиббса кристалла меньше, чем энергия Гиббса жидкой фазы. Если превращение происходит с небольшим изменением объема, то G= Е – ТS, где Е – полная энергия (внутренняя энергия фазы), Т – абсолютная температура, S – энтропия. Изменение энергии Гиббса металла в жидком и твердом состояниях в зависимости от температуры показано на рис. 13. Выше температуры ![]() более устойчив жидкий металл, имеющий меньший запас свободной энергии, а ниже этой температуры устойчив твердый металл.
более устойчив жидкий металл, имеющий меньший запас свободной энергии, а ниже этой температуры устойчив твердый металл.
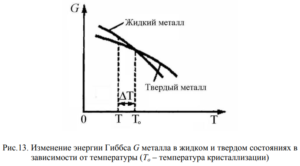
При температуре ![]() значения энергий Гиббса металла в жидком и твердом состояниях равны и обе фазы (жидкая и твердая) могут сосуществовать при этой температуре одновременно. Процесс кристаллизации при этой температуре еще не начинается и будет развиваться, если созданы условия, когда возникает разность энергий Гиббса
значения энергий Гиббса металла в жидком и твердом состояниях равны и обе фазы (жидкая и твердая) могут сосуществовать при этой температуре одновременно. Процесс кристаллизации при этой температуре еще не начинается и будет развиваться, если созданы условия, когда возникает разность энергий Гиббса ![]() образующаяся вследствие меньшей энергии Гиббса твердого металла по сравнению с жидким. Следовательно, процесс кристаллизации может протекать только при переохлаждении металла ниже равновесной температуры
образующаяся вследствие меньшей энергии Гиббса твердого металла по сравнению с жидким. Следовательно, процесс кристаллизации может протекать только при переохлаждении металла ниже равновесной температуры ![]() . Разница между равновесной
. Разница между равновесной ![]() и реальной температурой кристализации называется степенью переохлаждения
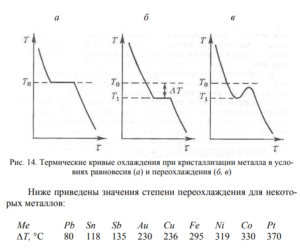
и реальной температурой кристализации называется степенью переохлаждения ![]() Степень пepeoxлаждения зависит от природы металла. Она увеличивается с повышением чистоты металла и ростом скорости охлаждения. Термические кривые, характеризующие процесс кристаллизации чистых металлов при охлаждении с разной скоростью, показаны на рис. 14.
Степень пepeoxлаждения зависит от природы металла. Она увеличивается с повышением чистоты металла и ростом скорости охлаждения. Термические кривые, характеризующие процесс кристаллизации чистых металлов при охлаждении с разной скоростью, показаны на рис. 14.
С увеличением скорости охлаждения степень переохлаждения возрастает (рис. 14, б, в) и процесс кристаллизации протекает при температурах, лежащих значительно ниже равновесной температуры кристаллизации. Обычная степень переохлаждения металлов при кристаллизации в производственных условиях колеблется от 10 до 30°С; при больших скоростях охлаждения она может достигать сотен градусов.
Плавление – процесс, обратный кристаллизации, происходит при температуре выше равновесной, т. е. при перегреве. Степень перегрева при плавлении металлов, как правило, не превышает нескольких градусов. Как указывалось выше, в жидкости имеются группировки атомов небольшого объема, в пределах которых расположение атомов вещества во многом аналогично их расположению в решетке кристалла. Эти группировки неустойчивы, они рассасываются и вновь появляются в жидкости.
При переохлаждении жидкости некоторые из них (наиболее крупные) становятся устойчивыми и способными к росту. Эти устойчивые группировки атомов называют центрами кристаллизации (зародышами). Образованию зародышей способствуют флуктуации энергии, т. е. отклонения энергии группировок атомов в отдельных зонах жидкого металла от некоторого среднего значения. Размер образовавшегося зародыша зависит от величины зоны флуктуации.
Появление центров изменяет термодинамический потенциал системы ![]() (рис. 15). С одной стороны, при переходе жидкости в кристаллическое состояние термодинамический потенциал уменьшается на
(рис. 15). С одной стороны, при переходе жидкости в кристаллическое состояние термодинамический потенциал уменьшается на ![]() . с другой − он увеличивается вследствие появления поверхности раздела между жидкостью и кристаллическим зародышем на величину, равную
. с другой − он увеличивается вследствие появления поверхности раздела между жидкостью и кристаллическим зародышем на величину, равную ![]()
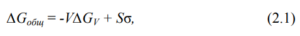
где ![]() − объем зародыша;
− объем зародыша; ![]() − удельная разность термодинамических потенциалов при переходе жидкости в кристаллическое состояние;
− удельная разность термодинамических потенциалов при переходе жидкости в кристаллическое состояние; ![]() − поверхность зародыша;
− поверхность зародыша; ![]() − удельное поверхностное натяжение на границе кристалл – жидкость. Если условно принять, что зародыш имеет сферическую форму, то общее уравнение термодинамического потенциала.
− удельное поверхностное натяжение на границе кристалл – жидкость. Если условно принять, что зародыш имеет сферическую форму, то общее уравнение термодинамического потенциала.
![]()
где ![]() – радиус зародыша; n – число зародышей. Из уравнения (2.2) следует, что зависимость изменения термодинамического потенциала от размера зародыша имеет максимум (рис. 15) при некотором значении
– радиус зародыша; n – число зародышей. Из уравнения (2.2) следует, что зависимость изменения термодинамического потенциала от размера зародыша имеет максимум (рис. 15) при некотором значении ![]() , названном критическим. Зародыши с размером больше критического вызывают уменьшение
, названном критическим. Зародыши с размером больше критического вызывают уменьшение ![]() и поэтому являются устойчивыми, способными к росту. Зародыши, имеющие размер меньше критического, нестабильны и растворяются
и поэтому являются устойчивыми, способными к росту. Зародыши, имеющие размер меньше критического, нестабильны и растворяются
в жидкости, поскольку вызывают увеличение ![]() . Величину критического зародыша можно определить из соотношения:
. Величину критического зародыша можно определить из соотношения:

Скорость процесса и окончательный размер кристаллов при затвердевании определяются соотношением между скоростью образования центров кристаллизации и скоростью роста. Первая измеряется числом зародышей, образующихся в единицу времени и единице объема ![]() , вторая – увеличением линейного размера растущего кристалла в единицу времени (мм/с). Оба процесса связаны с перемещениями атомов и зависят от температуры (рис. 16). Для металлов, которые в обычных условиях кристаллизации не склонны к большим переохлаждениям, как правило, характерны восходящие ветви кривых. При небольших степенях переохлаждения, когда зародыш критического размера велик, а скорость образования зародышей мала, при затвердевании формируется крупнокристаллическая структура. Небольшие степени переохлаждения достигаются при заливке жидкого металла в форму с низкой теплопроводностью (земляная, шамотовая) или в подогретую металлическую форму. Увеличение переохлаждения происходит при заливке жидкого металла в холодные металлические формы, а также при уменьшении толщины стенок отливки. Поскольку при этом скорость образования зародышей увеличивается более интенсивно, чем скорость их роста, получаются более мелкие кристаллы.
, вторая – увеличением линейного размера растущего кристалла в единицу времени (мм/с). Оба процесса связаны с перемещениями атомов и зависят от температуры (рис. 16). Для металлов, которые в обычных условиях кристаллизации не склонны к большим переохлаждениям, как правило, характерны восходящие ветви кривых. При небольших степенях переохлаждения, когда зародыш критического размера велик, а скорость образования зародышей мала, при затвердевании формируется крупнокристаллическая структура. Небольшие степени переохлаждения достигаются при заливке жидкого металла в форму с низкой теплопроводностью (земляная, шамотовая) или в подогретую металлическую форму. Увеличение переохлаждения происходит при заливке жидкого металла в холодные металлические формы, а также при уменьшении толщины стенок отливки. Поскольку при этом скорость образования зародышей увеличивается более интенсивно, чем скорость их роста, получаются более мелкие кристаллы.

Несамопроизвольная кристаллизация. В реальных условиях процессы кристаллизации и характер образующейся структуры в значительной мере зависят от имеющихся центров кристаллизации. Такими центрами, как правило, являются частицы тугоплавких неметаллических включений, оксидов, интерметаллических соединений, образуемых примесями. К началу кристаллизации центры находятся в жидком металле в виде твердых включений. При кристаллизации атомы металла откладываются на активированной поверхности примеси, как на готовом зародыше. Такая кристаллизация называется
несамопроизвольной, или гетерогенной. При несамопроизвольной кристаллизации роль зародышей могут играть и стенки формы.
В жидком металле могут присутствовать и растворенные примеси, которые также вызывают измельчение структуры. Адсорбируясь на поверхности зарождающихся кристаллов, они уменьшают поверхностное натяжение на границе раздела жидкость − твердая фаза и линейную скорость роста кристаллов. Из формулы (2.3) следует, что это способствует уменьшению ![]() и появлению новых зародышей, способных к росту. Примеси, понижающие поверхностное натяжение, называют поверхностно-активными. Измельчение структуры способствует улучшению механических свойств металла. На практике для измельчения структуры металлов и сплавов широко применяют технологическую операцию, называемую модифицированием. Она состоит во введении в жидкий сплав перед разливкой специальных добавок − модификаторов. В качестве последних используют поверхностно-активные вещества (например,
и появлению новых зародышей, способных к росту. Примеси, понижающие поверхностное натяжение, называют поверхностно-активными. Измельчение структуры способствует улучшению механических свойств металла. На практике для измельчения структуры металлов и сплавов широко применяют технологическую операцию, называемую модифицированием. Она состоит во введении в жидкий сплав перед разливкой специальных добавок − модификаторов. В качестве последних используют поверхностно-активные вещества (например,
бор в сталях, натрий в алюминии и его сплавах), а также элементы, образующие тугоплавкие тонкодисперсные частицы (например, титан, цирконий в алюминии и его сплавах; алюминий, титан в сталях).
Модификаторы добавляют в сплавы в количествах от тысячных до десятых долей процента. При увеличении температуры жидкого металла примеси, играющие роль дополнительных центров кристаллизации, растворяются или дезактивируются, поэтому повышение температуры жидкого металла перед разливкой приводит к укрупнению зерна при кристаллизации. Наоборот, подстуживание металла перед разливкой до температур, незначительно превышающих температуру плавления металла, способствует уменьшению размера зерна. Подстуживание эффективно при наличии примесей (или модификаторов), образующих фазы со структурным и размерным соответствием с основным металлом; в этом случае даже после значительных перегревов можно получить мелкое зерно, особенно если удлинить выдержку перед разливкой.
Строение слитка
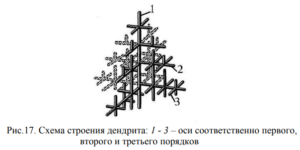
Форма и размер зерен, образующихся при кристаллизации, зависят от условий их роста, главным образом, от скорости и направления отвода теплоты и температуры жидкого металла, а также от содержания примесей. Рост зерна происходит по дендритной (древовидной) схеме (рис. 17). Установлено, что максимальная скорость роста кристаллов наблюдается по таким плоскостям и направлениям, которые имеют наибольшую плотность упаковки атомов. В результате вырастают длинные ветви, которые называются осями первого порядка. По мере роста на осях первого порядка появляются и начинают расти ветви
второго порядка, от которых ответвляются оси третьего порядка и т. д.
В последнюю очередь идет кристаллизация в участках между осями дендритов. Дендриты растут до тех пор, пока не соприкоснутся между собой. После этого окончательно заполняются межосные пространства, и дендриты превращаются в полновесные кристаллы с неправильной внешней огранкой. Такие кристаллы называют зернами или кристаллитами. При недостатке жидкого металла для заполнения межосных пространств (например, на открытой поверхности
слитка или в усадочной раковине) кристалл сохраняет дендритную форму. Такой дендрит обнаружен Д.К. Черновым на поверхности усадочной раковины стального слитка массой 100 т. На границах между зернами в участках между осями дендритов накапливаются примеси, появляются поры из-за усадки и трудностей подхода жидкого металла к фронту кристаллизации.
Условия отвода теплоты при кристаллизации значительно влияют на форму зерен. Кристаллы растут преимущественно в направлении,
обратном отводу теплоты, поэтому при направленном теплоотводе образуются столбчатые кристаллы. Если теплота от растущего кристалла отводится во всех трех направлениях с приблизительно одинаковой скоростью, формируются равноосные кристаллы. Структура слитка зависит от многих факторов, основные из которых следующие: количество и свойства примесей в чистом металле или легирующих элементов в сплаве, температура разливки, скорость
охлаждения при кристаллизации, а также конфигурация, температура, теплопроводность, состояние внутренней поверхности литейной
формы.
На рис. 18 приведены схемы макроструктур слитков, полученных в простой вертикальной металлической форме. Типичная структура слитка сплавов состоит из трех зон. Жидкий металл, прежде всего, переохлаждается в местах соприкосновения с холодными стенками формы. Большая степень переохлаждения
способствует образованию на поверхности слитка зоны 1 мелких равноосных кристаллов. Отсутствие направленного роста кристаллов этой зоны объясняется их случайной ориентацией, которая является причиной столкновения кристаллов и прекращения их роста. Ориентация кристаллов, в свою очередь, зависит от состояния поверхности формы (шероховатость, адсорбированные газы, влага) и наличия в жидком металле оксидов, неметаллических включений. Эта зона
очень тонка и не всегда различима невооруженным глазом.
Затем происходит преимущественный рост кристаллов, наиболее благоприятно ориентированных по отношению к теплоотводу. Так образуется
зона 2 столбчатых кристаллов, расположенных нормально к стенкам формы. Наконец, в середине слитка, где наблюдается наименьшая степень переохлаждения и не ощущается направленного отвода теплоты, образуются равноосные кристаллы больших размеров (зона 3). Применяя различные технологические приемы, можно изменить количественное соотношение зон или исключить из структуры слитка какую-либо зону вообще. Например, перегрев сплавов перед разливкой и быстрое охлаждение при кристаллизации приводят к формированию структуры, состоящей практически из одних столбчатых кристаллов (рис. 18, б). Такая структура называется транскристаллической. Подобную структуру имеют слитки очень чистых металлов. Зона столбчатых кристаллов характеризуется наибольшей плотностью, но в месте стыка столбчатых кристаллов собираются нерастворимые
примеси, и слитки с транскристаллической структурой часто растрескиваются при обработке давлением. Транскристаллическая структура, образовываясь в сварных швах, уменьшает их прочность.

Низкая температура разливки сплавов, продувка жидкого металла инертными газами, вибрация, модифицирование приводят к уменьшению и даже исчезновению зоны столбчатых кристаллов и получению слитков со структурой, состоящей из равноосных кристаллов (см. рис.18, в).
В верхней части слитка, которая затвердевает в последнюю очередь, концентрируется усадочная раковина. Под усадочной раковиной металл получается рыхлым, в нем содержится много усадочных пор. Часть слитка с усадочной раковиной и рыхлым металлом отрезают. Наконец, качественная структура формируется при непрерывной разливке. В этом случае жидкий металл поступает из печи через специальное устройство непосредственно в водоохлаждаемый кристаллизатор, а затвердевший металл непрерывно вытягивается с противоположного конца кристаллизатора.
При этом литой металл отличается высокой пластичностью и мелкозернистой структурой, приближаясь по качеству к деформированному металлу. Применение этого способа разливки позволяет автоматизировать и механизировать технологический процесс, сократить производственные площади, полностью исключить применение изложниц, разгрузить обжимное оборудование, облегчить труд обслуживающего персонала, увеличить выход годного металла вследствие заполнения жидким металлом усадочной раковины. Все это приводит к уменьшению себестоимости металла.
Слитки сплавов имеют неоднородный состав. Например, в стальных слитках по направлению от поверхности к центру и снизу вверх увеличивается концентрация углерода и вредных примесей − серы и фосфора. Химическая неоднородность по отдельным зонам слитка называется зональной ликвацией. Она отрицательно влияет на механические свойства. В реальных слитках, помимо зональной, встречаются и другие виды ликвации. Так, дендритная ликвация
свойственна сплавам с широким интервалом кристаллизации. Она характеризуется неодинаковым химическим составом по сечению зерна (дендрита). Центр зерна обогащен компонентом, повышающим солидус, к периферии его количество уменьшается.
Гравитационная ликвация образуется в результате разницы в плотностях твердой и жидкой фаз, а также при кристаллизации несмешивающихся жидких фаз. Это, например, свойственно антифрикционным сплавам олова с сурьмой и меди со свинцом. В зависимости от того, легче или тяжелее твердая фаза по сравнению с жидкой, она при кристаллизации соответственно всплывает на поверхность или опускается на дно отливки. Такое расслоение отливки (слитка) по
плотности недопустимо для антифрикционных сплавов, поскольку коэффициент трения в работающей паре в большой степени зависит как от особенности, так и однородности структуры. Для уменьшения гравитационной ликвации используют большие скорости охлаждения отливок (слитков).
Большое научное и практическое значение имеют монокристаллы. Монокристаллы отличаются минимальными структурными несовершенствами. Получение монокристаллов позволяет изучать свойства металлов, исключив влияние границ зерен. Применение в монокристаллическом состоянии германия и кремния высокой чистоты дает возможность использовать их полупроводниковые свойства и свести к минимуму неконтролируемые изменения электрических свойств.
Монокристаллы можно получить, если создать условия для роста кристалла только из одного центра кристаллизации. Существует несколько методов, в которых использован этот принцип. Важнейшими из них являются методы Бриджмена и Чохральского.

